日前����,Global Blood Therapeutics(GBT)公司宣布,美國(guó)FDA已經(jīng)接受該公司為口服鐮狀細(xì)胞貧血癥(SCD)療法voxelotor的新藥申請(qǐng)(NDA)���。同時(shí)����,F(xiàn)DA授予這一申請(qǐng)優(yōu)先審評(píng)資格���,預(yù)計(jì)將在明年2月26日前作出回復(fù)���。如果獲得批準(zhǔn),voxelotor將成為靶向血紅蛋白聚合過程的首款獲批療法���。值得注意的是����,FDA將使用加速批準(zhǔn)通路對(duì)voxelotor進(jìn)行審評(píng)���,這意味著voxelotor可以依靠替代終點(diǎn)的表現(xiàn)獲得批準(zhǔn)���。
SCD是由于表達(dá)血紅蛋白β鏈的基因出現(xiàn)突變引起的遺傳性血液疾病����。攜帶突變的基因會(huì)生成異常的鐮狀血紅蛋白(HbS)���。在脫氧狀態(tài)下���,HbS具有聚合或結(jié)合在一起的傾向,在紅細(xì)胞內(nèi)形成剛性棒狀結(jié)構(gòu)���。聚合的棒狀結(jié)構(gòu)使紅細(xì)胞變成鐮刀狀并喪失彈性���,可導(dǎo)致毛細(xì)血管和小血管的堵塞。從兒童期開始����,SCD患者由于血液無法順暢流向器官,出現(xiàn)不可預(yù)知和反復(fù)發(fā)作的嚴(yán)重疼痛危機(jī)���,常導(dǎo)致心理和身體殘疾����。阻斷的血流����,加上溶血性貧血(紅細(xì)胞的破壞)����,最終可能導(dǎo)致多器官損傷和早期死亡����。Voxelotor是一款每日口服一次的SCD創(chuàng)新療法,它通過增加血紅蛋白對(duì)氧的親和力達(dá)到療效���。由于氧合鐮狀血紅蛋白不會(huì)聚合���,voxelotor可防止紅細(xì)胞發(fā)生鐮狀改變以及血紅細(xì)胞的損毀。Voxelotor有著恢復(fù)正常血紅蛋白功能和改善氧氣輸送的潛力���。Voxelotor曾經(jīng)獲得美國(guó)FDA授予的突破性療法認(rèn)定����、孤兒藥資格����、快速通道資格和罕見兒科疾病認(rèn)定(rare pediatric disease designations)。
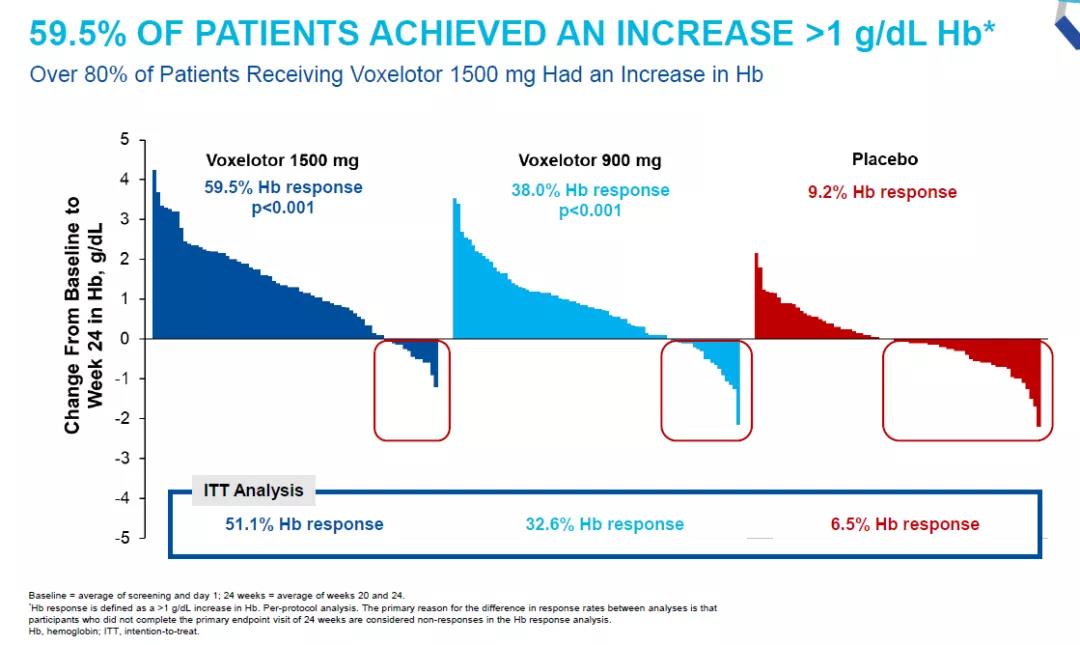
▲HOPE臨床試驗(yàn)療效結(jié)果(圖片來源:參考資料[2])
Voxelotor的申請(qǐng)是基于名為HOPE的3期臨床試驗(yàn)結(jié)果����。這一試驗(yàn)結(jié)果已經(jīng)在《新英格蘭醫(yī)學(xué)雜志》(The New England Journal of Medicine)上發(fā)表���。試驗(yàn)結(jié)果表明,接受劑量為1500 mg的voxelotor患者組中59.5%的患者血紅蛋白水平提高超過1 g/dL����。以往研究表明,血紅蛋白水平降低與負(fù)面臨床后果相關(guān)����,而將血紅蛋白水平提高1 g/dL可能顯著降低SCD患者臨床并發(fā)癥和死亡率。
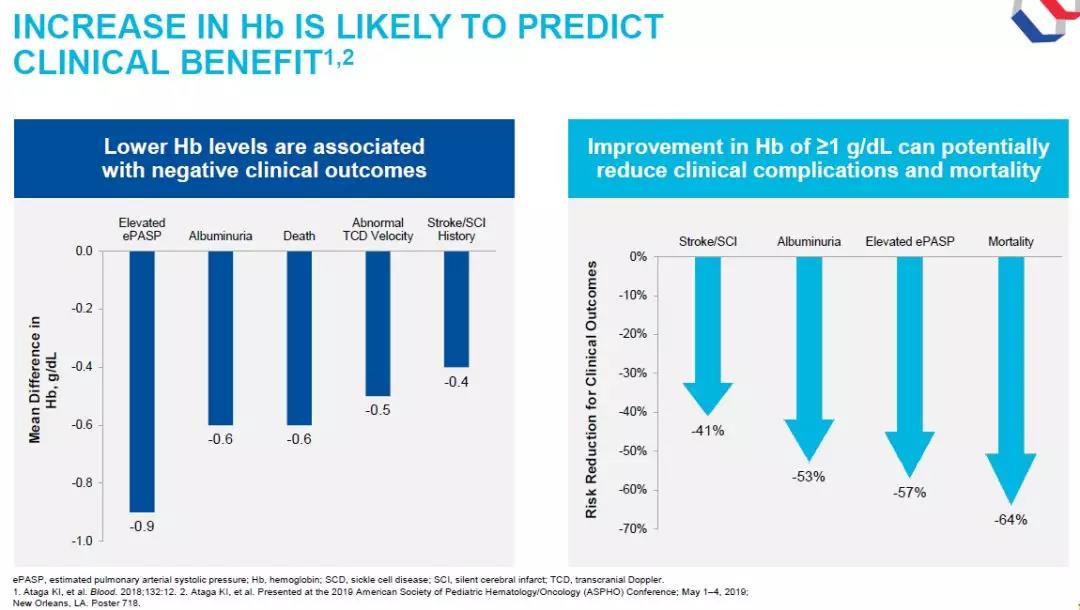
▲血紅蛋白水平上升可能預(yù)測(cè)臨床益處(圖片來源:參考資料[2])
FDA在接受這一新藥申請(qǐng)的同時(shí)表示���,目前不準(zhǔn)備召開咨詢委員會(huì)會(huì)議����,對(duì)voxelotor的新藥申請(qǐng)進(jìn)行討論���。“FDA接受voxelotor的新藥申請(qǐng)并且授予其優(yōu)先審評(píng)資格���,是這一在研療法開發(fā)過程中的重要里程碑。它體現(xiàn)了將這款創(chuàng)新療法盡早帶給SCD患者的重要性,”GBT公司總裁兼首席執(zhí)行官Ted W. Love博士說:“我們期待與FDA緊密合作���,希望能夠早日改變SCD的治療模式���。”
參考資料:
[1] GBT Announces U.S. Food and Drug Administration Acceptance of New Drug Application and Priority Review for Voxelotor for the Treatment of Sickle Cell Disease. Retrieved September 7, 2019, from https://www.globenewswire.com/news-release/2019/09/05/1911462/0/en/GBT-Announces-U-S-Food-and-Drug-Administration-Acceptance-of-New-Drug-Application-and-Priority-Review-for-Voxelotor-for-the-Treatment-of-Sickle-Cell-Disease.
[2] EHA 2019 CORPORATE UPDATE. Retrieved September 7, 2019, from https://ir.gbt.com/static-files/fe2a8a7a-ddd9-4bf5-a5ff-700746f1bca3




