今日,禮來(lái)(Lilly)公司宣布��,美國(guó)FDA批準(zhǔn)該公司開(kāi)發(fā)的Reyvow(lasmiditan)片劑上市����,作為急性療法治療有先兆或無(wú)先兆成年偏頭痛患者���。Reyvow具有獨(dú)特的作用機(jī)制���,是FDA批準(zhǔn)的首款也是唯一款血清素(5-HT)1F受體激動(dòng)劑�。新聞稿指出���,這是20多年來(lái)�����,F(xiàn)DA批準(zhǔn)急性治療偏頭痛的第一種新藥物類型���。
偏頭痛是一種以嚴(yán)重頭痛發(fā)作為特征的神經(jīng)疾病,伴隨頭痛的其它癥狀包括惡心和對(duì)聲光敏感���。超過(guò)10%的世界人口受到偏頭痛的困擾�����,而婦女受到偏頭痛影響的幾率是男性的三倍�����。雖然目前有多種治療和預(yù)防偏頭痛的藥物�,但是它仍然沒(méi)有得到足夠的重視和治療。據(jù)統(tǒng)計(jì)���,近40%的偏頭痛患者在接受第一種急性療法治療的時(shí)候反應(yīng)不足��。禮來(lái)公司開(kāi)發(fā)的Reyvow是一種創(chuàng)新口服5-HT1F受體激動(dòng)劑���。它能夠與5-HT1F受體以高親和力相結(jié)合。Reyvow(lasmiditan)是獲得FDA批準(zhǔn)的首款“地坦”(ditans)類藥物�����。目前常見(jiàn)的偏頭痛急性療法為曲坦類(triptans)藥物�,這些藥物是5-HT1B/1D受體激動(dòng)劑,雖然它們?cè)诰徑馄^痛方面有著顯著的療效��,然而激活5-HT1B受體亞型能夠產(chǎn)生血管收縮效應(yīng)�,帶來(lái)其它副作用��。Reyvow不會(huì)激活5-HT1B受體�����,因此不會(huì)產(chǎn)生血管收縮效應(yīng)。對(duì)于患有心血管疾病或處于心血管疾病風(fēng)險(xiǎn)中的偏頭痛患者來(lái)說(shuō)更為安全���。
▲Lasmiditan分子結(jié)構(gòu)式(圖片來(lái)源:Anypodetos [Public domain])
Reyvow的療效在兩項(xiàng)隨機(jī)雙盲�,含安慰劑對(duì)照的3期臨床試驗(yàn)(SAMURAI和SPARTAN)中得到驗(yàn)證�。3177名有偏頭痛歷史的患者參加了這兩項(xiàng)臨床試驗(yàn)。試驗(yàn)結(jié)果表明�����,Reyvow組與安慰劑組相比���,在服藥2個(gè)小時(shí)后患者頭痛完全消失的比例顯著提高�,Reyvow同時(shí)顯著消除其它最困擾患者的偏頭痛癥狀(惡心和聲光敏感)�。值得一提的是,在對(duì)曲坦類藥物反應(yīng)不足的患者亞群中����,Reyvow也能夠產(chǎn)生良好的效果。
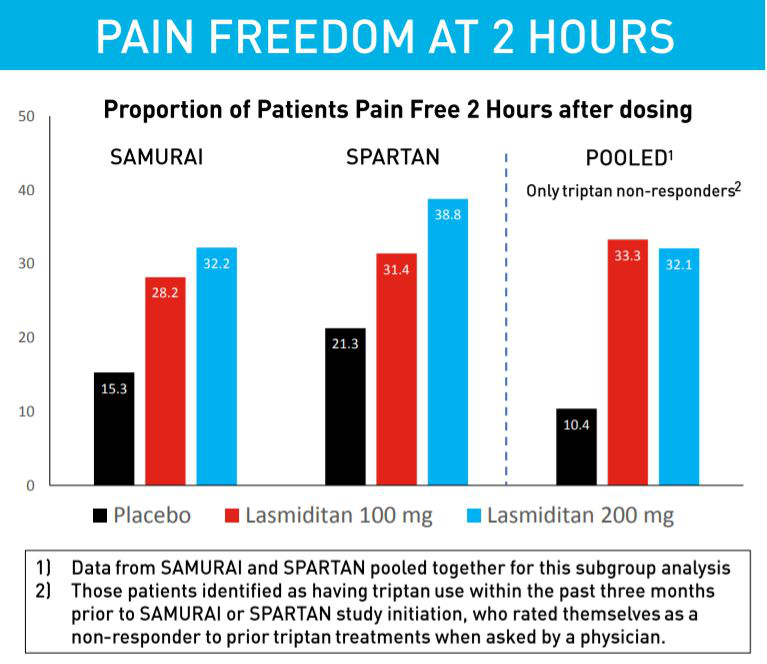
▲Reyvow在3期臨床試驗(yàn)中的部分療效結(jié)果(圖片來(lái)源:參考資料[3])
“上百萬(wàn)偏頭痛患者每天要與無(wú)法消除的疼痛和其它偏頭痛癥狀作斗爭(zhēng)���。在偏頭痛急性治療方面仍然存在很大未竟需求��。今天的批準(zhǔn)讓我們感到非常自豪���,禮來(lái)將繼續(xù)為偏頭痛患者造福��,”禮來(lái)生物醫(yī)藥神經(jīng)科開(kāi)發(fā)副總裁Gudarz Davar博士說(shuō):“在治療偏頭痛方面我們有了新的期望值�,無(wú)痛是偏頭痛患者和醫(yī)師們的治療目標(biāo)��。禮來(lái)將繼續(xù)開(kāi)發(fā)創(chuàng)新產(chǎn)品���,為偏頭痛患者提供新的治療選擇���。”
參考資料:
[1] FDA approves new treatment for patients with migraine. Retrieved October 11, 2019, from https://www.prnewswire.com/news-releases/fda-approves-new-treatment-for-patients-with-migraine-300937273.html
[2] Lilly's REYVOW? (lasmiditan), The First and Only Medicine in a New Class of Acute Treatment for Migraine, Receives FDA Approval. Retrieved October 11, 2019, from https://www.prnewswire.com/news-releases/lillys-reyvow-lasmiditan-the-first-and-only-medicine-in-a-new-class-of-acute-treatment-for-migraine-receives-fda-approval-300937322.html
[3] 2018 Investment Community Meeting. Retrieved October 11, 2019, from https://investor.lilly.com/static-files/e1cc74de-ada5-4ae4-b5a4-7ecf0969197d[4] Lilly Submits New Drug Application to the FDA for Lasmiditan for Acute Treatment of Migraine, Receives Breakthrough Therapy Designation for Emgality? (galcanezumab-gnlm) for Prevention of Episodic Cluster Headache. Retrieved October 11, 2019, from https://investor.lilly.com/news-releases/news-release-details/lilly-submits-new-drug-application-fda-lasmiditan-acute[5] Therapeutic novelties in migraine: new drugs, new hope? Retrieved October 11, 2019, from https://doi.org/10.1186/s10194-019-0974-3




