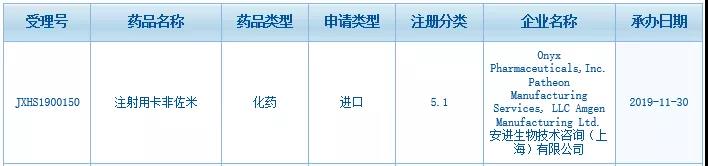
根據(jù)中國國家藥監(jiān)局藥品審評中心(CDE)最新公示�,安進公司(Amgen)旗下的注射用卡非佐米(carfilzomib)在中國的上市申請已獲得CDE受理���。這是一款蛋白酶體抑制劑���,用于治療多發(fā)性骨髓瘤。值得一提的是��,今年11月初��,百濟神州與安進達成全球腫瘤戰(zhàn)略合作關(guān)系�,將在中國開發(fā)和商業(yè)化多款安進已獲批的腫瘤產(chǎn)品���,還將在全球范圍內(nèi)共同開發(fā)20款抗腫瘤藥物��。其中在中國商業(yè)化合作部分就包括這款藥物——KYPROLIS?(carfilzomib)���,它正在中國開發(fā)后期用于治療多發(fā)性骨髓瘤。
細胞內(nèi)的蛋白酶體(proteasomes)能夠分解受損或不再需要的蛋白���,它對細胞的正常功能和生長都有重要的作用��。Carfilzomib是安進公司開發(fā)的第二代蛋白酶體抑制劑��,它的作用機制在于���,通過阻斷蛋白酶體分解蛋白的功能���,導致細胞內(nèi)蛋白的過度積累。在有些細胞中���,carfilzomib會導致細胞死亡�。由于骨髓瘤細胞中含有大量異常蛋白���,因此�,carfilzomib引發(fā)骨髓瘤細胞死亡的效果尤其明顯�。

2016年,carfilzomib獲得美國FDA批準�,可以作為單一療法或者與dexamethasone或dexamethasone + lenalidomide構(gòu)成組合療法治療復發(fā)或難治性MM患者。它同時也在澳大利亞�、加拿大、中國香港��、日本、韓國���、瑞士���、俄羅斯等國家和地區(qū)獲得批準上市。自獲批以來���,全球有接近8萬名患者已經(jīng)接受過carfilzomib的治療��。
在一項名為ASPIRE的臨床3期試驗中��,792名復發(fā)或難治性MM患者接受了KRd或Rd的治療�。這些患者已經(jīng)接受過1~3種其它療法的治療�。試驗結(jié)果表明,接受KRd療法患者組的平均OS為48.3個月���,接受Rd療法患者組的平均OS為40.4個月。KRd療法能夠?qū)S延長7.9個月�。在只接受過一次其它療法治療的患者亞群中,KRd療法的療效更好���,與Rd療法相比能夠?qū)⑵骄鵒S延長11.4個月���。患者的無進展生存期(PFS)數(shù)據(jù)已經(jīng)在去年發(fā)表���,KRd與Rd療法相比,能夠?qū)FS延長8.7個月���。多發(fā)性骨髓瘤(multiple myeloma, MM)是一種血液系統(tǒng)惡性腫瘤�,無法治愈且復發(fā)率很高��。它是由于骨髓中的漿細胞癌變導致的罕見但是危及生命的血癌�,占癌癥總數(shù)的2%左右。它的一個重要特征是會反復出現(xiàn)緩解和復發(fā)��。我們期待這款藥物早日獲批上市���,造福更多多發(fā)性骨髓瘤患者���。



