9月22日���,貝達藥業(yè)宣布,其自主研發(fā)的EGFR-TKI鹽酸?�?颂婺幔▌P美納)的新適應癥上市申請獲得中國國家藥品監(jiān)督管理局(NMPA)受理���,用于術后輔助治療��。研究顯示:?�?颂婺嵊糜诜切〖毎伟∟SCLC)患者術后輔助治療能顯著延長患者無病生存期���,同時安全性更優(yōu)。此前�,?��?颂婺嵋言谥袊@批用于治療非小細胞肺癌。
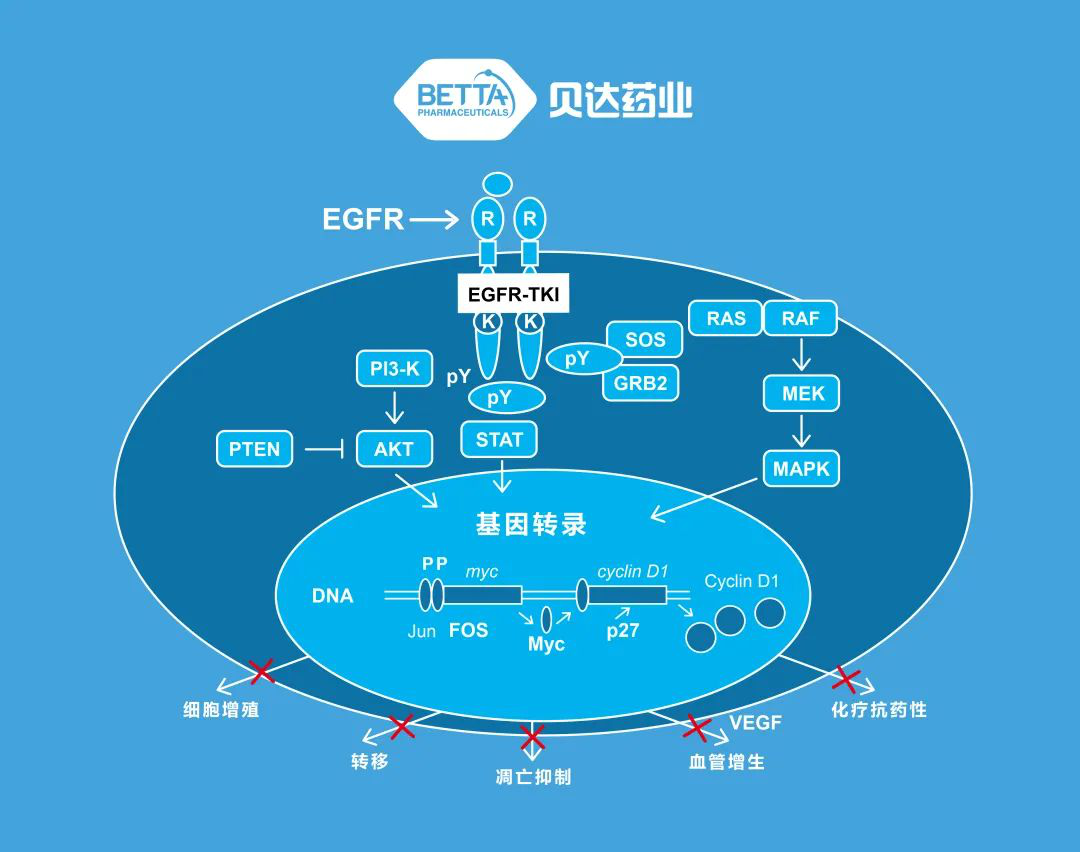
表皮生長因子受體(EGFR)高表達于多種類型的腫瘤細胞��,與其配體表皮生長因子(EGF)結合后��,激活EGFR細胞漿部分的激酶活性����,通過不同的信號傳導途徑調節(jié)多種基因的轉錄,從而調控細胞的增殖�、分化、凋亡等���。表皮生長因子受體酪氨酸激酶抑制劑(EGFR-TKI)能特異、競爭性地結合EGFR激酶功能區(qū)的ATP結合位點����,抑制其激酶活性從而阻斷癌細胞增殖、轉移等相關信號的傳導���。?�?颂婺崾秦愡_藥業(yè)歷時近十年自主研發(fā)的一種強效���、高選擇性的口服EGFR-TKI��,屬于1.1類創(chuàng)新藥����。根據新聞稿�,該藥是中國第一個自主創(chuàng)新的小分子靶向抗癌新藥。2011年6月�,埃克替尼在中國獲批上市����,用于非小細胞肺癌的二/三線的治療。2014年11月�����,?�?颂婺嵩俅潍@得批準��,單藥適用于治療EGFR基因具有敏感突變的局部晚期或轉移性非小細胞肺癌患者的一線治療���。自上市以來���,?����?颂婺嵋呀浕菁俺^26萬名晚期肺癌患者����。▲??颂婺?/span>作用機理(圖片來源:參考資料[1])本次埃克替尼獲得NMPA受理的是一項新適應癥申請——用于術后輔助治療����。在一項名為EVIDENCE的研究中,比較了??颂婺崤c標準輔助化療針對II-IIIA期肺癌EGFR突變患者術后輔助治療的效果。截止2020年6月的數(shù)據顯示:在療效方面�����,?����?颂婺嶂委熃M對比標準輔助化療組��,患者中位無病生存期(DFS)為46.95個月 vs 22.11個月���;3年DFS率為63.88% vs 32.47%���;在安全性方面,??颂婺嶂委熃M不良反應發(fā)生率明顯低于標準輔助化療組,3級及以上不良反應發(fā)生率為4.49% ����,標準化療組為59.71%。研究認為���,綜合來看��,?����?颂婺嵊糜?em style="margin: 0px; padding: 0px; max-width: 100%; box-sizing: border-box !important; word-wrap: break-word !important;">EGFR基因敏感突變的NSCLC患者術后輔助治療的療效優(yōu)于標準輔助化療����,能顯著延長患者無病生存期,同時安全性更優(yōu)�。根據新聞稿,??颂婺嵘鲜泻箝_展了80多項臨床學術研究,包括一線治療研究�����、肺癌伴腦轉移研究��、EGFR狀態(tài)不明患者研究���、EGFR21L858R外顯子敏感突變加量研究�、與化療聯(lián)合的研究等����。祝賀埃克替尼的新適應上市申請獲受理���,也希望該藥的其它研究順利進行��,造福更多病患���。