2021年7月29日,羅氏集團(tuán)(Roche)旗下基因泰克(Genentech)宣布��,美國FDA已授予其雙特異性抗體faricimab的生物制品許可申請(BLA)優(yōu)先審評資格,用于治療濕性(新生血管性)年齡相關(guān)性黃斑變性(AMD)和糖尿病性黃斑水腫(DME)。美國FDA也已接受該藥用于治療糖尿病視網(wǎng)膜病變(DR)的申請。新聞稿指出�����,一旦獲批�,faricimab將成為首款作用于眼睛的雙特異性抗體。該藥同時靶向阻斷兩條致病關(guān)鍵通路——血管生成素-2(Ang-2)和血管內(nèi)皮生長因子-A(VEGF-A)�,這兩種通路通過破壞血管的穩(wěn)定性,驅(qū)動許多可導(dǎo)致視力喪失的視網(wǎng)膜疾病�����。

該項BLA申請基于4項3期臨床試驗的積極結(jié)果�����,分別為針對濕性AMD患者的TENAYA和LUCERNE試驗�����,以及針對DME患者的YOSEMITE和RHINE試驗�。所有試驗均達(dá)到其主要終點��,顯示與每兩個月給藥一次的當(dāng)前標(biāo)準(zhǔn)治療相比�,每4個月給藥一次faricimab達(dá)到非劣效性標(biāo)準(zhǔn)的視力獲益。并且�����,大約一半適合延長faricimab給藥間隔的濕性AMD或DME患者,在接受治療第一年時就只需每4個月接受一次給藥���。新聞稿指出����,faricimab是首個在濕性AMD和DME的3期臨床試驗中���,達(dá)到這么長持久性的眼部注射藥物�。安全性方面�,在所有4項試驗中,faricimab通常耐受良好����,未發(fā)現(xiàn)新/非預(yù)期安全性信號。
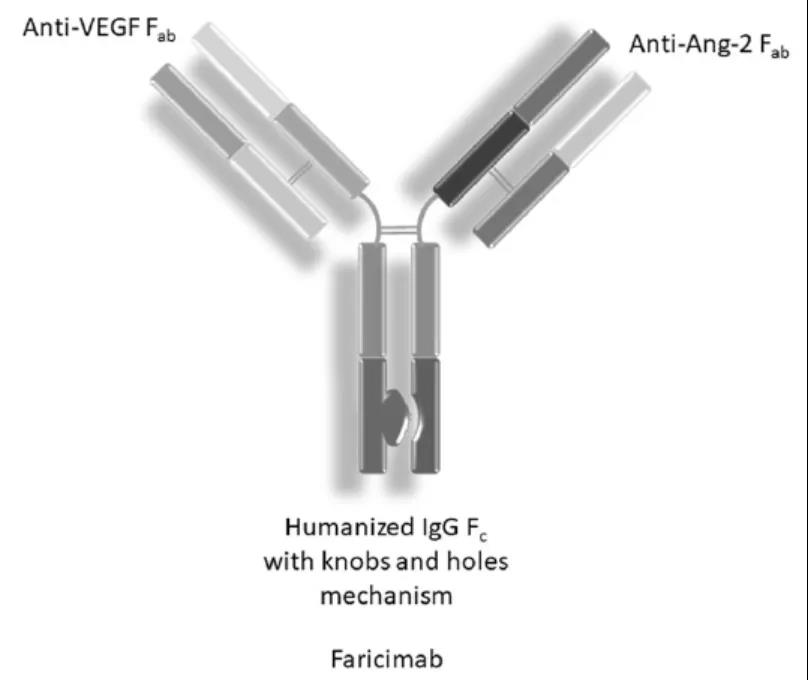
▲Faricimab結(jié)構(gòu)示意圖(圖片來源:參考資料[2])
AMD是60歲及以上人群致盲的主要原因��。濕性AMD是一種晚期疾病����,可導(dǎo)致快速和嚴(yán)重的視力喪失。濕性AMD是由異常血管向黃斑部生長所致����。這些血管滲漏液體和血液�,引起瘢痕組織生長��,破壞中央視網(wǎng)膜���,導(dǎo)致視力在數(shù)月至數(shù)年內(nèi)惡化��。DME是糖尿病視網(wǎng)膜病變的并發(fā)癥�,后者是20~74歲成年人致盲的主要原因�����。DME是血管損傷和新血管形成���,導(dǎo)致血液和/或液體滲漏到視網(wǎng)膜所致。“如果獲批��,faricimab將成為首款靶向驅(qū)動視網(wǎng)膜疾病兩個關(guān)鍵通路的新型眼藥��。它有望提供持久的視力改善�,并且眼部注射給藥次數(shù)比目前的標(biāo)準(zhǔn)治療更少、更方便��。”羅氏與基因泰克首席醫(yī)學(xué)官兼全球產(chǎn)品開發(fā)負(fù)責(zé)人Levi Garraway博士表示��,“我們希望faricimab為數(shù)百萬濕性AMD和DME患者提供一種新的治療選擇�����?��!?/span>
參考資料:
[1] FDA Accepts Application for Genentech’s Faricimab for the Treatment of Wet Age-Related Macular Degeneration (AMD) and Diabetic Macular Edema (DME). Retrieved July 29, 2021, from https://www.businesswire.com/news/home/20210728006055/en
[2] Sharma et al., (2019). Faricimab: expanding horizon beyond VEGF. Eye, https://doi.org/10.1038/s41433-019-0670-1



