Cybrexa Therapeutics今日宣布�����,臨床前癌癥模型證明�����,在研肽偶聯(lián)藥物(PDC)CBX-12能增強(qiáng)免疫檢查點(diǎn)抑制劑的效果�����。目前�����,Cybrexa正在進(jìn)行一項(xiàng)1/2期臨床試驗(yàn),以確定CBX-12的耐受性和安全性�����。該公司的初步重點(diǎn)將針對(duì)HER2過(guò)度表達(dá)的卵巢癌和小細(xì)胞肺癌(SCLC)患者�����。
免疫檢查點(diǎn)抑制劑與化療聯(lián)用是多種實(shí)體瘤的標(biāo)準(zhǔn)療法�����,但與化療相關(guān)的骨髓抑制會(huì)降低免疫療法的療效�����。并且�����,由于其對(duì)正常細(xì)胞的影響�����,化療還會(huì)產(chǎn)生各種毒副作用�����。而靶向化療�����,如抗體偶聯(lián)藥物(ADC)則受限于只能治療表達(dá)高水平靶抗原的腫瘤�����。那么�����,有沒有什么辦法�����,既能特異性地靶向廣泛的腫瘤類型�����,又能避免毒性呢�����?所有腫瘤的特征之一就是酸性微環(huán)境。而CBX-12可將一種強(qiáng)效的細(xì)胞毒素exatecan�����,特異性遞送至低pH值環(huán)境的細(xì)胞中�����。它利用了一種低pH插入肽(pHLIP)的獨(dú)特變體�����,低pH值改變這種多肽的構(gòu)象�����,將exatecan遞送至細(xì)胞內(nèi)�����。這種選擇性靶向腫瘤細(xì)胞的作用機(jī)制�����,避免了與療法攻擊健康細(xì)胞相關(guān)的毒性�����。臨床前癌癥模型顯示�����,CBX-12不會(huì)像化療一樣誘導(dǎo)骨髓抑制�����。
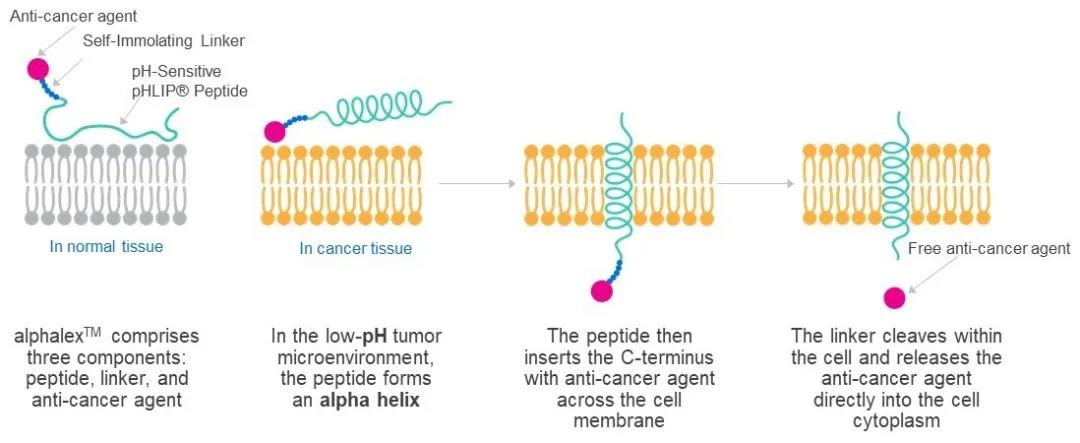
▲利用低pH插入肽將抗癌藥物遞送到腫瘤細(xì)胞的機(jī)制(圖片來(lái)源:Cybrexa公司官網(wǎng))研究人員使用結(jié)直腸癌小鼠模型�����,進(jìn)一步評(píng)估了CBX-12對(duì)PD-1和CTLA4免疫檢查點(diǎn)抑制劑療效的影響�����。實(shí)驗(yàn)結(jié)果顯示�����,與單獨(dú)使用免疫檢查點(diǎn)抑制劑的小鼠相比�����,接受聯(lián)合療法治療的小鼠腫瘤生長(zhǎng)顯著延緩,存活率提高�����,并表現(xiàn)出完全的腫瘤消退�����。具體而言�����,CBX-12與PD-1抑制劑聯(lián)用延緩小鼠腫瘤生長(zhǎng)4倍�����,與CTLA4抑制劑聯(lián)用延緩腫瘤生長(zhǎng)10倍�����。不僅如此�����,經(jīng)歷腫瘤完全消退的小鼠還表現(xiàn)出長(zhǎng)期的免疫記憶。而將CBX-12處理的腫瘤細(xì)胞注射到小鼠體內(nèi)�����,可導(dǎo)致抗腫瘤免疫應(yīng)答�����,表明CBX-12誘導(dǎo)了免疫原性細(xì)胞死亡�����。“抗體偶聯(lián)藥物受限于腫瘤需要表達(dá)高水平的靶抗原�����。而CBX-12的新穎之處在于它靶向酸性環(huán)境�����,這是所有腫瘤的普遍特征�����。因此�����,我們能夠在更廣泛的患者群體中�����,選擇性地將一種強(qiáng)效抗癌藥物遞送至腫瘤細(xì)胞�����?����!盋ybrexa的生物學(xué)副主任Sophia Gayle博士表示�����,“我們的研究結(jié)果表明�����,將CBX-12與免疫檢查點(diǎn)抑制結(jié)合�����,可以將免疫療法的療效擴(kuò)展到正常情況下對(duì)它們不產(chǎn)生應(yīng)答的腫瘤?����?紤]到約80%的患者對(duì)免疫檢查點(diǎn)抑制劑單藥治療沒有反應(yīng)�����,這可以使廣泛的患者受益�����。Gayle博士也指出�����,由于實(shí)驗(yàn)都在臨床前模型中進(jìn)行�����,未來(lái)還需要進(jìn)行額外的研究以了解這種組合療法對(duì)患者的影響�����。



