今日,諾華(Novartis)宣布���,美國FDA已經(jīng)批準該公司的靶向放射性配體療法Pluvicto(lutetium Lu 177 vipivotide tetraxetan,曾用名177Lu-PSMA-617)上市,用于治療前列腺特異性膜抗原(PSMA)陽性轉(zhuǎn)移性去勢抵抗性前列腺癌(mCRPC)患者���。他們已經(jīng)接受過基于紫杉烷的化療和雄激素受體信號通路抑制劑治療���。新聞稿指出,Pluvicto是首款FDA批準用于治療這類mCRPC患者的靶向放射配體療法���。它將同位素療法與靶向化合物結(jié)合在一起���。
近年來,放射性藥物成為腫瘤精準治療領(lǐng)域的一個重要方向���。諾華的Pluvicto將結(jié)合PSMA的小分子化合物與放射性同位素連接在一起���。它可與表達PSMA的前列腺癌細胞結(jié)合,放射性同位素釋放的輻射能量會損害腫瘤細胞���,引發(fā)細胞死亡���。PSMA在超過80%的前列腺癌患者中高度表達���。由于Pluvicto釋放的輻射只能在很短距離里起作用���,因此限制了藥物對周圍健康細胞的損害���。這款療法此前獲得了FDA授予的突破性療法認定,它的新藥申請也獲得了FDA授予的優(yōu)先審評資格���。
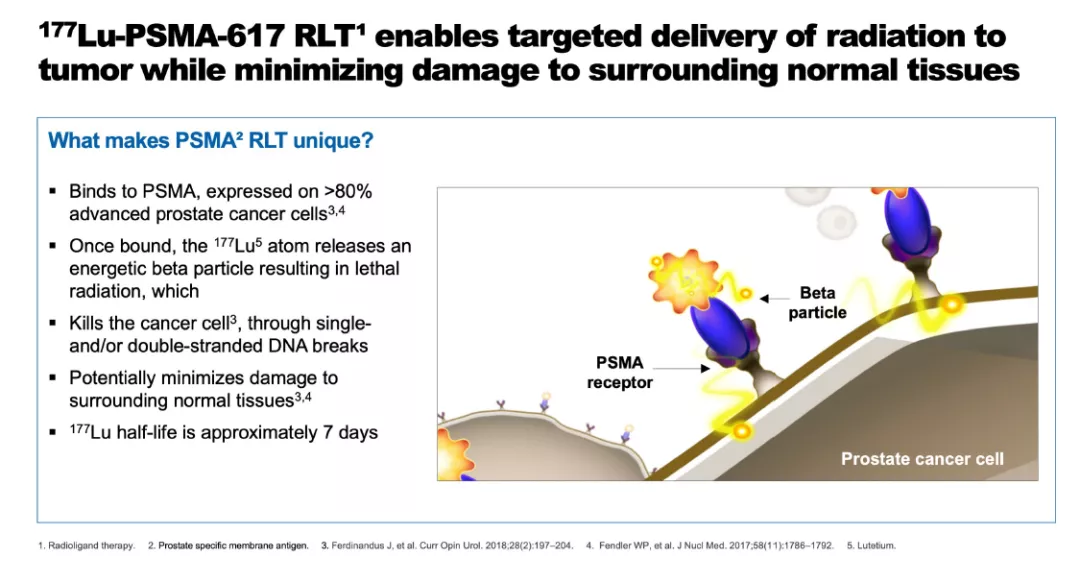
▲Pluvicto(177Lu-PSMA-617)療法簡介(圖片來源:諾華官網(wǎng))這一批準是基于一項關(guān)鍵性3期臨床試驗的積極結(jié)果���。試驗結(jié)果顯示,與標準治療相比���,添加Pluvicto將患者的死亡風險降低38%���,Pluvicto同時顯著降低患者出現(xiàn)放射學(xué)疾病進展或死亡的風險。而且���,在基線攜帶可評估疾病的患者中���,Pluvicto組的總緩解率為30%,標準治療對照組這一數(shù)值為2%���。“Pluvicto的獲批對mCRPC患者來說是個重要臨床進展���,它可以顯著改善這些治療選擇有限的患者的生存率���。” 杜蘭癌癥中心(Tulane Cancer Center)的Oliver Sartor博士說���,“Pluvicto是前列腺癌精準醫(yī)療發(fā)展的一大進步���。”
參考資料:
[1] Novartis PluvictoTM approved by FDA as first targeted radioligand therapy for treatment of progressive, PSMA positive metastatic castration-resistant prostate cancer. Retrieved March 23, 2022, from https://www.globenewswire.com/news-release/2022/03/23/2408996/0/en/Novartis-PluvictoTM-approved-by-FDA-as-first-targeted-radioligand-therapy-for-treatment-of-progressive-PSMA-positive-metastatic-castration-resistant-prostate-cancer.html
[2] Pluvicto label. Retrieved March 23, 2022, from https://www.accessdata.fda.gov/drugsatfda_docs/label/2022/215833s000lbl.pdf



